

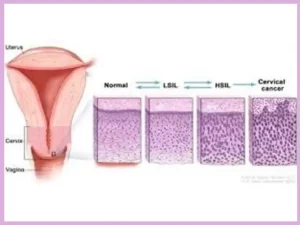
Як змінилась класифікація захворювань шийки матки: від CIN до сучасних стандартів
Морфологічні критеріі Крона та неспецифічного виразкового коліту

Знайомство з роботою лікаря-цитоморфолога лабораторії ПтМЦД

Інтраопераційне гістологічне експрес-дослідження
Цитологія

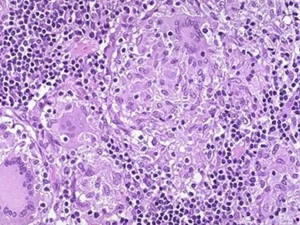
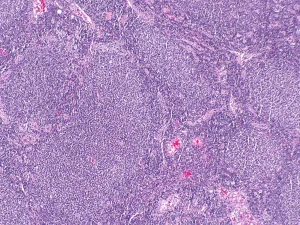
Клінічний випадок: Фолікулярна лімфома

Цитологія
